
(1)
Isótopos são átomos que possuem o mesmo número de prótons (consequentemente, o mesmo número atômico). Esse é fácil porque a palavra “isótopo” tem um “p” de “prótons”. Como não existem dois elementos químicos com o mesmo número de prótons, substâncias isótopas são formadas por átomos do mesmo elemento químico. Essas substâncias apresentam propriedades químicas iguais e propriedades físicas diferentes.
Isótonos, por sua vez, são átomos que possuem o mesmo número de nêutrons. O “n” de “nêutrons” no meio de “isótonos” também facilita a associação. Como o número de prótons, nesse caso, é diferente, o número atômico e o número de massa também serão.
Isóbaros, por fim, são átomos com o mesmo número de massa (A). Você pode associar o “a” no meio da palavra “isóbaros” com o “A” que representa o número de massa, mas mesmo que você não lembre que o número de massa é representado pela letra A, fazendo as associações anteriores você saberá, por exclusão, que isobaria tem relação com o número de massa.
Sabendo que o número de massa é igual e o número de prótons é diferente (já que os elementos não são isótopos), pode-se concluir que o número de nêutrons também será diferente.
| Semelhança Atômica | Número de Prótons (Z) | Número de massa (A) | Número de nêutrons (n) | Número de elétrons (e) |
| ISÓTOPOS | = | ≠ | ≠ | ≠ |
| ISÓBAROS | ≠ | = | ≠ | ≠ |
| ISÓTONOS | ≠ | ≠ | = | ≠ |
| ISOELETRÔNICOS | ≠ | ≠ | ≠ | = |
Atividades
1) Observe a tabela abaixo:
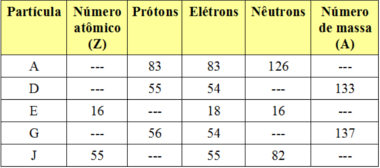
Tabela de exercício sobre isótopos e isóbaros
Baseado nos dados acima, indique quais são, respectivamente, isótopos e isóbaros entre si:
Isótopos/ Isóbaros:
a) D e J; G e J.
b) D e G; A e E.
c) A e J; E e G.
d) G e J; A e D.
e) E e G; G e J.
2) Certo átomo possui 17 prótons, 20 nêutrons e 17 elétrons. Qual dos átomos representados abaixo é seu isótono?
a) 19K40
b) 20Ca42
c) 21Sc42
d) 20Ca40
e) 22Ti43
3) O átomo “X” é isótono do átomo 25Mn55 e isoeletrônico do íon 2860Ni2+. Com base nisso, indique o número de massa do átomo “X”:
a) 56.
b) 55.
c) 58.
d) 60.
e) 62.
4) (UA-AM) Em relação à isotopia, isobaria e isotonia, podemos afirmar que:
a) isótonos são entidades químicas que possuem o mesmo número de nêutrons.
b) isóbaros são entidades químicas que possuem o mesmo número de prótons.
c) isótopos são entidades químicas que possuem o mesmo número de massa.
d) são relações que dizem respeito ao núcleo e à eletrosfera do átomo.
e) são relações que dizem respeito apenas à eletrosfera do átomo.
Resposta Questão 1
Alternativa “a”.
Preenchendo completamente a tabela temos:
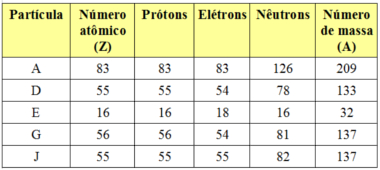
Exercício sobre isótopos e isóbaros
Os isótopos são os que possuem o mesmo número atômico ou quantidade de prótons. Olhando na tabela vemos que o D e o J são isótopos. Já os isóbaros são os que possuem o mesmo número de massa, que é o caso do G e do J.
Resposta Questão 2
Alternativa “d”.
Os isótonos possuem o mesmo número de nêutrons, que é encontrado pela subtração do número de massa (canto superior esquerdo) pelo número de prótons (canto inferior esquerdo). Assim, temos:
20Ca40 = 40 – 20 = 20.
Resposta Questão 3
Alternativa “a”.
Se o átomo “X” é isótono do átomo 25Mn55, isso significa que ele possui 30 nêutrons (55-25). E se ele é isoeletrônico do íon 2860Ni2+, quer dizer que ele possui 26 elétrons (28 – 2). Visto que está no estado fundamental, o átomo “X” também possui 26 prótons. Assim, para descobrir o seu número de massa, basta somar os prótons com os nêutrons: A = 30 + 26 = 56.
Resposta Questão 4
Alternativa “a”.
a) Correta.
b) Incorreta. Isóbaros são entidades químicas que possuem o mesmo número de massa.
c) Incorreta. Isótopos são entidades químicas que possuem o mesmo número de prótons.
d) Incorreta. São relações que dizem respeito apenas ao número do átomo.
e) Incorreta. Vide item anterior.




Nenhum comentário:
Postar um comentário